PANCREAS ECTOPIQUE :
Le pancréas ectopique (ou aberrant, ou hétérotopie pancréatique) se définit par la présence de tissu pancréatique en situation anormale, sans rapport anatomique avec la glande principale.
Son incidence est estimée entre 0,5 et 14 % sur les séries autopsiques(1) , mais est probablement sous-estimée du fait de son caractère le plus souvent asymptomatique.
Les localisations habituelles sont représentées par le duodénum (30-35% des cas), l’estomac (30%) et le jéjunum (15%)(2). D’autres sites ont été décrits mais sont exeptionnels (vésicule biliaire, hile splénique, voie biliaire principale, oesophage, rate, mésentère, épiploon, diverticule de Meckel).
Le pancréas aberrant peut être complet associant tissu exocrine (canalaire et acineux) et endocrine, ou ne contenir que l’un de ces éléments. Il est la plupart du temps situé dans la sous muqueuse, plus rarement dans la musculeuse.
La pathogénèse(3) impliquerait soit une séparation puis une migration de tissu pancréatique lors de la rotation des bourgeons ventral et dorsal, soit une mauvaise différenciation de la muqueuse.
Le pancréas aberrant est le plus souvent asymptomatique, de découverte fortuite lors d’examens complémentaires ou sur des séries autopsiques, ou est responsable de douleurs pseudo-ulcéreuses. Il peut d’une manière générale être sujet aux mêmes pathologies (pancréatite aiguë, chronique, tumeurs) que le pancréas orthotopique.
Les modes de découverte en imagerie concernent 2 formes macroscopiquement différentes : la dystrophie kystique sur pancréas aberrant et la forme nodulaire, de topographie essentiellement gastrique.
- Dystrophie Kystique sur Pancréas Aberrant (DKPA) :
La DKPA de la paroi duodénale survient rarement isolément (25% des cas). Elle est fréquemment associée à une pancréatite chronique touchant la glande principale et le pancréas aberrant (75%)(4). Celui ci est situé dans la paroi supéro-interne du 2ème duodénum. Macroscopiquement il existe une infiltration oedémateuse de la paroi duodénale qui est épaissie, associée à la présence de formations kystiques souvent multiples. Il s’agit le plus souvent d’un homme de 50 ans aux antécédents d’éthylisme, présentant une douleur (pancréatique ou ulcéreuse) associée à une occlusion haute (vomissements, amaigrissement).
Le diagnostic à l’imagerie est évoqué devant(5; 6) :
- un épaississement de la paroi duodénale
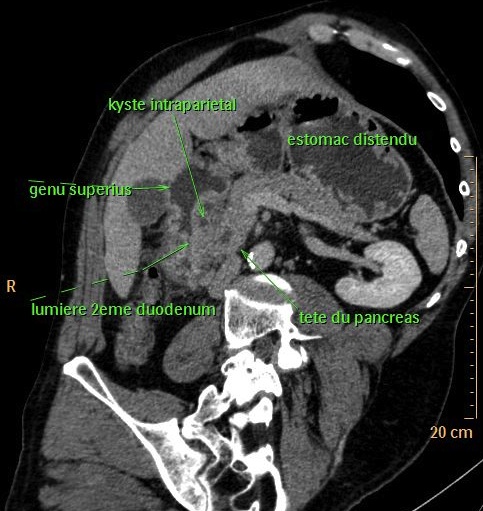
- l’existence de plusieurs kystes de petite taille dans la paroi digestive (image tdm, image irmt2, image bili-irm)
- une tuméfaction pancréatique céphalique
- une sténose d’allure extrinsèque de la partie supérieure et interne du D2
On recherchera également des lésions de pancréatite chronique associées (cf), un déplacement de l’artère gastro-duodénale vers la gauche par la lésion kystique intra-duodénale (au temps artériel de l’injection), une dilatation et une stase gatrique d’amont.
L’IRM est excellente pour détecter les formations kystiques en franc hypersignal T2 et pour en préciser leur situation intrapariétale duodénale(6). La CPRM montre l’absence d’anomalie canalaire pancréatique (kystes indépendants).
L’échoendoscopie est l’examen le plus performant pour établir le diagnostic en montrant un épaississement hyperéchogène diffus de la paroi duodénale qui contient des formations kystiques limitées par la musculeuse(6; 7).
Les diagnostics différentiels sont représentés par les pseudokystes pancréatiques (formations macrokystiques, uniques ou en faible nombre, à distance des épisodes de pancréatite aiguë et sans épaississement pariétal digestif), les tumeurs primitives du duodénum et les duplications digestives.
- Pancréas ectopiques (PE) gastriques(3)
Les PE gastriques sont plus rares que les DKPA duodénales et moins souvent symptomatiques. Il s’agit de lésions sous muqueuses, refoulant les plis gastriques, généralement de petite taille (<3cm) et d’aspect nodulaire. Le réhaussement est identique à celui de la glande pancréatique mais variable selon la composante (rehaussement le plus similaire au pancréas dans les formes acinaires). L’antre gastrique est le siège le plus fréquent. Le diagnostic différentiel avec une GIST (tumeur stromale gatro-intestinale) gastrique est parfois difficile(8). Les autres diagnostics différentiels à évoquer sont les léiomyomes, les tumeurs endocrines et les lymphomes gastriques (gamme diagnostique des lésions sous muqueuses gastriques).
Références bibliographiques :
1. Potet F, Duclert N. [Cystic dystrophy on aberrant pancreas of the duodenal wall]. Arch Fr Mal App Dig 1970 mars;59(4):223-238.
2. Basili E, Laugier R. [Cystic dystrophy in heterotopic pancreas of the duodenal wall]. Gastroenterol. Clin. Biol. 2003 déc;27(12):1110-1115.
3. Orry X, Ropion Michaux H, Gervaise A, Fairise A, Laurent V, Régent D. Imagerie des pancréas ectopiques: aspect en imagerie, formes particulières, diagnostics différentiels. JFR 2011 (poster électronique).
4. Pessaux P, Lada P, Etienne S, Tuech J-J, Lermite E, Brehant O, Triau S, Arnaud J-P. Duodenopancreatectomy for cystic dystrophy in heterotopic pancreas of the duodenal wall. Gastroenterol. Clin. Biol. 2006 janv;30(1):24-28.
5. Procacci C, Graziani R, Zamboni G, Cavallini G, Pederzoli P, Guarise A, Bogina G, Biasiutti C, Carbognin G, Bergamo-Andreis IA, Pistolesi GF. Cystic dystrophy of the duodenal wall: radiologic findings. Radiology 1997 déc;205(3):741-747.
6. Galloro G, Napolitano V, Magno L, Diamantis G, Nardone G, Bruno M, Mollica C, Persico G. Diagnosis and therapeutic management of cystic dystrophy of the duodenal wall in heterotopic pancreas. A case report and revision of the literature. JOP 2008;9(6):725-732.
7. Jouannaud V, Coutarel P, Tossou H, Butel J, Vitte R-L, Skinazi F, Blazquez M, Hagège H, Bories C, Rocher P, Belloula D, Latrive J-P, Meurisse J-J, Eugène C, Dellion M-P, Cadranel J-F, Pariente A. Cystic dystrophy of the duodenal wall associated with chronic alcoholic pancreatitis. Clinical features, diagnostic procedures and therapeutic management in a retrospective multicenter series of 23 patients. Gastroenterol. Clin. Biol. 2006 avr;30(4):580-586.
8. Kim JY, Lee JM, Kim KW, Park HS, Choi JY, Kim SH, Kim MA, Lee JY, Han JK, Choi BI. Ectopic pancreas: CT findings with emphasis on differentiation from small gastrointestinal stromal tumor and leiomyoma. Radiology 2009 juill;252(1):92-100.
| < Précédent | Suivant > |
|---|





